Pengertian Larutan Elektrolit Kuat dan Elektrolit Lemah Beserta Perbedaannya – Kimia menjadi mata pelajaran yang dianggap sulit oleh siswa. Asumsi ini muncul bukan tanpa alasan karena di dalamnya kita harus menghafal berbagai macam teori serta rumus kompleks. Larutan elektrolit bisa kita manfaatkan untuk menyusun sebuah konduktor arus listrik. Kita bisa membaginya menjadi dua jenis yakni larutan elektrolit lemah dan arutan elektrolit kuat. Masing-masing tentunya memiliki pengertian, unsur, serta manfafat yang berbeda satu sama lain.
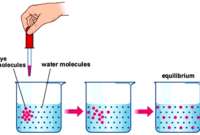
Lantas apa itu larutan elektrolit dalam mapel kimia? Larutan elektrolit ialah jenis larutan yang dapat menghantarkan arus listrik. Sebelumnya para peneliti telah melakukan eksperimen mengenai larutan elektrolit. Anda dapat memperhatikan gambar di bawah ini sebagai ilustrasi.
|
|
| Larutan Elektrolit |
Berdasarkan gambar di atas dapat kita lihat hasil pengujian mengenai larutan elektrolit. Perhatikan gambar diatas, terdapat salah satu lampu yang menyala. Lampu yang menyala tersebut membuktikan bahwa larutan elektrolit dapat menghantarkan arus listrik.
Kemudian larutan ini memiliki tiga kategori yaitu elektronik kuat (terlihat pada lampu yang menyala terang), elektrolit lemah (terlihat pada lampu yang menyala redup), dan non elektrolit (terlihat pada lampu yang tidak menyala sama sekali). Nah pada kesempatan kali ini saya akan membahas tentang pengertian larutan elektrolit kuat, pengertian larutan elektrolit lemah beserta perbedaan larutan elektrolit kuat dan larutan elektrolit lemah. Untuk lebih jelasnya dapat anda simak di bawah ini.
Pengertian Larutan Elektrolit Kuat dan Elektrolit Lemah Beserta Perbedaannya
Dalam konteks pendidikan, materi yang membahas perbedaan larutan elektrolit kuat dan lemah bisa kita jumpai ketika berada di bangku sekolah menengah. Kita bisa mempelajarinya secara mandiri karena materi yang mencakup pengertian, unsur, serta rumusnya tertulis rapi di buku pedoman kimia. Meski guru sudah menyampaikan pembahasan secara intensif namun masih banyak siswa yang belum menguasai materi tersebut.
Hasilnya, saat guru meminta menyebutkan definisi larutan elektrolit maka siswa pun tak bisa menjawabnya. Padahal materi satu ini sering muncul sebagai butir soal ujian yang notabenya sangat menyulitkan. Maka dari itu, saya ingin membahas lebih dalam tentang pengertian dan perbedaan larutan elektrolit kuat dan lemath secara lengkap.
Baca juga : Sifat Sifat Unsur, Senyawa dan Campuran Beserta Contoh Lengkap
Larutan elektrolit kuat seperti larutan HCl mengandung ion yang cukup banyak sehingga dapat membuat lampu menyala terang. Kemudian larutan elektrolit lemah seperti asam asetat mengandung ion yang sedikit sehingga hanya dapat membuat lampu menyala redup. Sedangkan untuk larutan non elektrolit seperti sukrosa tidak mengandung ion apapun sehingga tidak bisa menghantarkan arus listrik.
Larutan Elektrolit Kuat
Pengertian larutan elektrolit kuat adalah senyawa yang apabila dilarutkan kedalam air akan mengalami proses ionisasi dengan sempurna. Jenis larutan ini berasal dari beberapa jenis larutan seperti basa kuat, garam yang dapat larut di air dan asam kuat. Contoh elektrolit kuat ialah garam NaCl dimana didalamnya terdapat hasil larutan seperti anion dan kation. Apabila garam NaCl ini dilarutkan ke dalam air maka akan menghasilkan ion Na+ serta Cl-.
Kemudian adapula contoh larutan elektrolit kuat yang berasal dari asam kuat. Asam kuat ini berasal dari penelitian Arrhenius tentang Asam dan Basa. Berdasarkan pendapatnya, Asam merupakan jenis senyawa yang apabila dilarutkan ke dalam air akan menghasilkan ion H+. Maka dari itu saat zat asam seperti H2SO4, HCl, dan HNO3 larut ke dalam air maka masing masing atomnya akan terionisasi. Proses ionisasi asam yang sempurna ini menunjukkan karakteristik asam kuat beserta larutan elektrolit kuat.
Dalam pengertian larutan elektrolit kuat terdapat jenis elektrolit yang berasal dari basa kuat. Jenis elektrolit ini mengandung ion Hidroksida. Ketika basa kuat dilarutkan kedalam air, maka proses ionisasinya akan terjadi secara sempurna. Seperti halnya yang terjadi pada asam kuat. Namun basa kuat menghasilkan ion OH- dan bukan ion H+. Di bawah ini terdapat ciri ciri larutan elektrolit kuat yang meliputi :
- Dapat menghantarkan listrik dengan baik dan kuat.
- Proses ionisasinya sempurna.
- Derajat ionisasi (a) atau tetapannya ialah a = 1.
- Apabla dilakukan pengujian larutan elektrolit kuat maka akan muncul gelembung gas yang banyak serta lampu akan menyala terang.
Larutan Elektrolit Lemah
Pengertian larutan elektrolit lemah adalah senyawa yang apabila dilarutkan kedalam air akan mengalami proses ionisasi sebagian. Maka dari itu larutan elektrolit lemah hanya akan menghasilkan ion yang sedikit didalam air. Larutan ini berasal dari dua jenis larutan yakni basa lemah dan asam lemah. Contoh larutan elektrolit lemah yang berasal asam lemah yaitu HC2K3O2 (Asam Asetat). Ketika asam asetat ini dilarutkan ke dalam air maka tidak akan mengalami proses ionisasi dengan sempurna. Hal ini dikarenakan molekul yang terionisasi menjadi ion hanya 1% dari larutan airnya.
Baca juga : Penjelasan Konfigurasi Elektron Lengkap
Pada definisi larutan elektrolit lemah di atas ada pula jenis larutan yang asalnya dari basa lemah. Jika basa lemah dilarutkan ke dala air maka tidak bisa terionisasi dengan sempurna. Maka dari itu basa lemah hanya dapat menghantarkan arus lstrik yang sedikit. Contoh basa lemah yang termasuk ke dalam elektrolit lemah yaitu NH3 (Ammonua). Di bawah ini terdapat ciri ciri larutan elektrolit lemah yang meliputi :
- Dapat menghantarkan listrik yang lemah atau kurang baik
- Proses ionisasinya sebagian.
- Derajat ionisasi (a) atau tetapannya ialah 0 < a < 1.
- Apabla dilakukan pengujian larutan elektrolit lemah, maka akan muncul gelembung gas yang sedikit serta lampu akan menyala redup.
Perbedaan Larutan Elektrolit Kuat dan Lemah
Meskipun sudah mendapat pembahasan sesuai porsinya tapi kita tak bisa menampik fakta bahwa masih banya siswa tak paham cara membedakan kedua jenis larutan tersebut. Hal ini menurut saya cukup lumrah karena perbedaan larutan elektrolit kuat dan lemah tidak kasat mata. Kalian perlu melakukan beberapa analisa sebelum bisa menilainya. Selanjutnya saya akan membahas tentang perbedaan larutan elektrolit kuat dan larutan elektrolit lemah. Berikut penjelasannya:
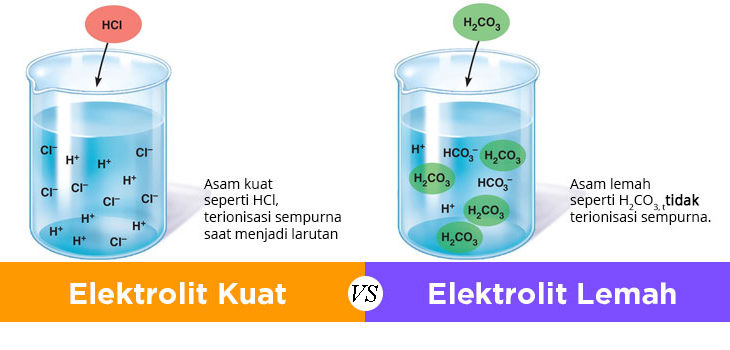
Elektrolit Kuat
Apa saja ciri-ciri elektrolit kuat? inilah pertanyaan yang sering diajukan oleh siswa sekolah menengah. Untuk membedakan jenis larutan yang mampu menghantar arus listrik maka kita harus mengenal karaktersitiknya terlebih dahulu.
- Proses ionisasinya sempurna.
- Larutannya mengandung ion yang banyak.
- Penghantar listrik yang kuat.
- Mempunyai derajat ionisasi yang mencapai nilai 1.
- Dapat menyalakan lampu dengan terang.
Baca juga : Pengertian, Teori, Sifat Asam dan Basa
Elektrolit Lemah
Sama seperti saudaranya, kita bisa mengidentifikasi elektrolit lemah lewat beberapa ciri-ciri khusus. Sebenarnya karakteristik tersebut sudah tertuang pada buku pedoman kimia. Tapi dalam sesi ini saya akan menjabarkan poin-poinnya:
- Proses ionisasinya tidak sempurna atau sebagian.
- Larutannya mengandung ion yang sedikit.
- Penghantar listrik yang lemah.
- Mempunyai derajat ionisasi yang kurang dari 1.
- Dapat menyalakan lampu dengan redup.
Demikianlah penjelasan mengenai pengertian larutan elektrolit kuat, pengertian larutan elektrolit lemah beserta perbedaan larutan elektrolit kuat dan larutan elektrolit lemah. Semoga artikel ini dapat bermanfaat. Terima kasih.