Pengertian Destilasi, Prinsip Kerja, Macam Macam, dan Tujuannya – Penemuan destilasi pertama kali pada abad pertama Masehi oleh Kimiawan Yunani. Dikala itu perkembangannya dipicu oleh tingginya permintaan spritus Hypathia dari Alexandria. Sekitar abad ke 4, proses destilasi ini secara akurat berhasil digambarkan oleh Zosimus dari Alexandria. Kemudian penemuan bentuk modern destilasi pertama kali oleh ahli kimia Islam di masa kekhalifahan Abbasiah, khususnya Al-Raazi untuk memisahkan alkohol menjadi senyawa murni dengan menggunakan alat alembik.
Metode destilasi paling penting diterapkan dengan cara memisahkan minyak mentah menjadi bagian khusus seperti untuk pembangkit listrik, pemanas, transportasi dan sebagainya. Apakah anda tahu apa pengertian destilasi itu? Bagaimana prinsip kerja destilasi? Apa tujuan destilasi? Apa saja macam macam destilasi?
Proses destilasi ini secara umum dapat kita temukan dalam pembelajaran kimia. Proses ini menyuling senyawa tertentu menjadi senyawa murni untuk keperluan tertentu. Materi ini sebenarnya telah dipelajari ketika di bangku sekolah. Namun ada beberapa siswa yang masih belum paham apa itu destilasi. Nah pada kesempatan kali ini saya akan menjelaskan tentang pengertian destilasi, prinsip kerja destilasi, macam macam destilasi, dan tujuan destilasi. Untuk lebih jelasnya dapat anda simak di bawah ini.
Pengertian Destilasi, Prinsip Kerja, Macam Macam, dan Tujuannya
Destilasi pada umumnya dapat dinamakan dengan penyulingan atau distilasi. Destilasi merupakan suatu metode yang berguna sebagai pemisah bahan kimia berdasarkan kemudahan atau perbedaan kecepatan dalam volatilitas bahan maupun menguap. Proses ini bertujuan agar cairan dapat terpisah dari zat padat dan membuat zat cair menjadi murni terhadap titik didihnya.
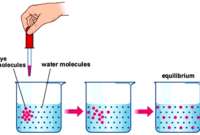
Seperti yang kita tahu bahwa dalam proses penyulingan terdapat zat yang bercampur hingga kemudian di didihkan agar dapat menguap dan berikutnya uap ini kembali di didihkan menjadi bentuk cairan. Bagaimana jika titik didih zat lebih sedikit? Jika hal ini terjadi makamzat tersebut akan di uapkan terlebih dahulu meskipun titik didihnya lebih sedikit.
Dari penjelasan ini apakah anda sudah mengerti apa itu destilasi? Jika masih belum, maka perhatikan artikel tentang pengertian destilasi, prinsip kerja destilasi, macam macam destilasi, dan tujuan destilasi yang akan saya bahas ini. Berikut penjelasan selengkapnya:
Baca juga : Perbedaan Unsur, Senyawa dan Campuran Terlengkap
Pengertian Destilasi
Destilasi adalah cara memisahkan zat cair dengan campurannya berdasarkan kemampuan zat dalam menguap atau perbedaan titik didihnya. Misalnya memisahkan sebuah campuran yang fasanya berbeda seperti zat cair dan padat, maka hanya cukup menggunakan penyaring atau filter saja untuk memisahkan kedua zat tadi.
Jika campuran berbentuk zat cair yang homogen, maka komponen campuran itu tidak dapat dipisahkan dengan cara menyaringnya saja. Komponen ini dapat dipisahkan dengan salah satu cara seperti proses destilasi ini yang disesuaikan dengan perbedaan titik didihnya. Tetapi ketika sebuah campuran berasal dari dua komponen yang berbeda titik didihnya dan bahkan cukup jauh berbeda, maka proses destilasi ini dapat digunakan untuk memisahkannya sesuai dengan syarat tertentu.
Contoh destilasi tersebut adalah pemisahan campuran antara air dan etanol yang besar titik didihnya berbeda. Air mempunyai titik didih yang besarnya 100°C, sedangkan titik didih etanol adalah 77°C saja. Kedua unsur campuran tersebut dapat dipisahkan dengan menggunakan serangkaian proses dalam destilasi tersebut.
Prinsip Kerja Destilasi
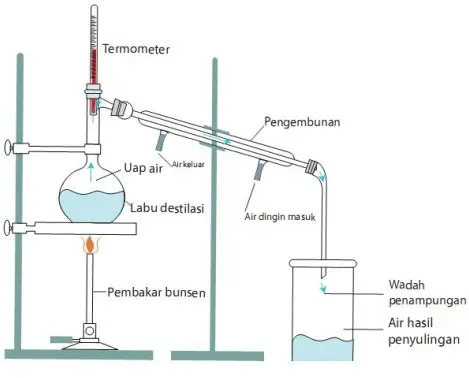
Setelah menjelaskan pengertian destilasi di atas, selanjutnya saya akan membahas tentang prinsip kerja destilasi. Destilasi dapat diartikan sebagai sebuah proses pemurnian senyawa padat yakni proses penguapan senyawa cair yang terlebih dahulu dilakukan melalui pemanasan, kemudian uap yang diperoleh diembunkan dan ditampung dalam wadah terpisah sampai memperoleh senyawa cair murni atau destilat.
Pemisahan destilasi pada dasarnya melalui perbedaan titik didih cairan yang memiliki tekanan tertentu. Pemisahan destilasi ini berhubungan dengan penguapan differensial dari sebuah campuran cairan yang disertai dengan penampungan uapan material melalui pengembunan dan pendinginan. Dengan destilasi ini, cairan dapat diubah menjadi uap dan didinginkan kembali menjadi cairan lagi. Destilasi tersebut juga memiliki unit operasi yang berbentuk metode untuk memisahklan komponen pada campuran atau larutan sesuai dengan distribusi komponen fasa air dan fasa uap.
Opersai pemisahan komponen dengan destilasi memiliki syarat utama yaitu komposisi uap harus berbeda dengan komposisi cairan agar larutan larutannya seimbang dan cukup untuk bisa menguap. Proses destilasi memiliki beberapa tahapan seperti di bawah ini:
- Pemindahan pelarut berbentuk uap dari suatu cairan atau evaporasi.
- Memisahkan uap dengan cairan dalam kolom dan memisahkan komponen yang lebih rendah titik didihnya dan mudah menguap dengan komponen lain yang volatilnya kurang.
- Melakukan kondensasi uap dan memperoleh fraksi pelarut yang volatilnya lebih.
Tujuan Destilasi
Setelah menjelaskan pengertian destilasi dan prinsip kerja destilasi di atas, selanjutnya saya akan membahas tentang tujuan proses destilasi. Destilasi bertujuan untuk memurnikan cairan dengan zat padatnya dan memurnikan bentuk cairnya melalui titik didih di dalamnya. Kemudian uap yang dihasilkan ini akan keluar dalam bentuk uap bebas. Hasil jatuhnya konsentrat ini dinamakan dengan destilat, sedangkan bagian cair yang tidak dapat menguap dinamakan residu. Bagian cair yang tidak menguap ini dapat dikentalkan menggunakan proses evaporasi.
Baca juga : 45 Contoh Perubahan Kimia Beserta Proses dan Penjelasannya
Macam Macam Destilasi
Destilasi dapat dibagi menjadi beberapa jenis seperti di bawah ini:
Destilasi Sederhana
Destilasi sederhana atau destilasi biasa dapat dilakukan dengan menaikkan suhu sehingga letak tekanan uapnya di luar tekanan atmosfer atau titik didih normal atau cairan. Dasar pemisahan destilasi campuran adalah perbedaan jauhnya titik didih atau salah satu komponen yang sifatnya volatil. Jika terjadi pemisahan campuran, maka titik didih yang dimiliki komponen tersebut akan lebih rendah dan lebih dulu melakukan penguapan. Selain perbedaan titik didih, adapula perbedaan kevolatilan yakni kecenderungan sebuah substansi yang dijadikan gas.
Kita dapat melakukan proses destilasi ini menggunakan tekanan atmoster. Destilasi tersebut berguna untuk memisahkan alkohol dengan campuran air. Di bawah ini terdapat susunan rangkaian yang menggunakan alat destilasi biasa yaitu:
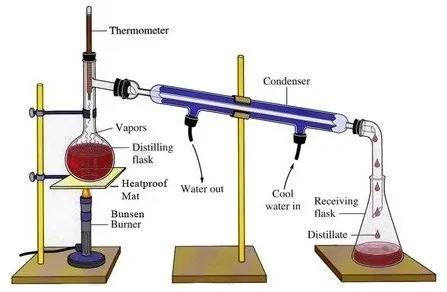
Destilasi Bertingkat
Macam destilasi selanjutnya adalah destilasi bertingkat atau destilasi berfraksi atau fungsi destilasi fraksionasi. Pengertian destilasi bertingkat adalah destilasi yang berguna untuk memisahkan komponen cair berdasarkan perbedaan titik didihnya sebanyak dua larutan atau lebih. Destilasi ini dapat digunakan untuk campuran yang titik didihnya berbeda kurang dari 20°C dan bekerja dalam tekanan rendah atau ditekanan atmosfer.
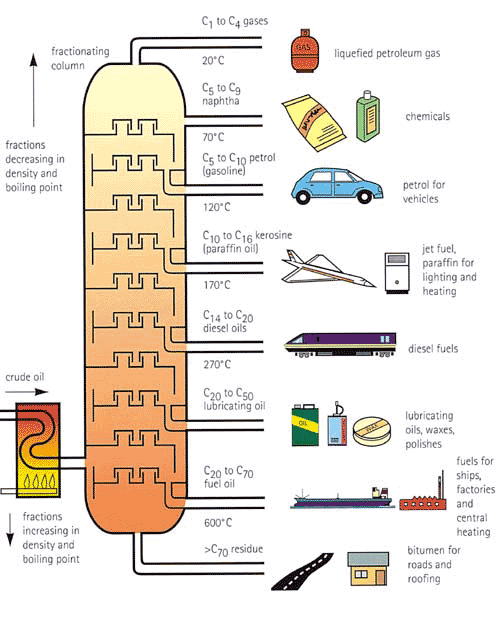
Kita dapat mengaplikasikan teknik destilasi ini di dunia industri minyak mentah yaitu sebagai pemisah komponen yang terdapat dalam minyak tanah tersebut. Destilasi fraksionasi berbeda dengan destilasi biasa dalam hal kolom fraksionasinya. Dalam kolom tersebut ada pemanasan yang terjadi secara bertahap di setiap platnya meskipun berbeda suhu. Tujuan proses pemanasan yang berbeda ini adalah untuk memurnikan destilat lebih yang berasal dari plat dibawahnya.
Destilasi Uap
Macam destilasi selanjutnya adalah destilasi uap. Pengertian destilasi uap adalah destilasi yang digunakan dalam campuran senyawa dan memiliki titik didih 200°C atau lebih. Senyawa yang diuapkan dengan jenis destilasi ini akan memiliki suhu terdekat 100°C disertai dengan air mendidih atau uap di tekanan atmosfer. Destilasi uap bersifat fundamental yakni mendestilasi campuran senyawa yang letaknya di bawah titik didih masing masing senyawa campuran.
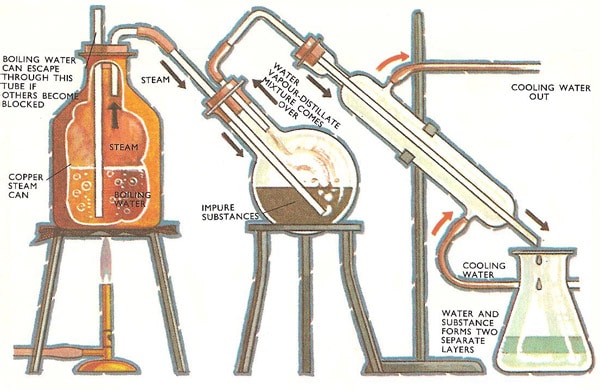
Destilasi uap juga dapat digunakan pada campuran yang tidak terlarut dalam air di semua temperatur, tetapi destilasi ini dapat dilakukan dengan air. Biasanya pengaplikasian jenis destilasi ini terjadi dalam pengekstrakkan sejumlah produk yang alami. Misalnya minyak sitrus yang asalnya dari lemon atau jeruk, minyak ecalyptus dari ecaluyptus serta minyak parfum dari tumbuhan.
Destilasi Vakum
Macam destilasi selanjutnya adalah destilasi vakum. Pengertian destilasi vakum adalah destilasi yang digunakan pada senyawa yang tidak stabil tetapi mendekati titik didihnya atau terdekomposisi sampai melebihi 150°C. Selain itu destilasi vakum juga digunakan sebagai pemisah dua komponen yang sangat tinggi titik didihnya. Metode destilasi vakum tersebut dilakukan dengan menurunkan tekanan permukaan sampai lebih rendah 1 atm, sehingga lebih rendah titik didihnya. Suhu yang digunakan dalam proses ini memang tidak terlalu tinggi.
Destilasi Azetrop
Destilasi azetrop adalah jenis destilasi yang digunakan untuk menguapkan zat cair tanpa merubah komposisi. Kegunaan destilasi ini adalah sebagai pemisah dua campuran atau lebih yang sulit terpisah. Proses destilasi ini menggunakan tekanan tinggi atau senyawa lain yang digunakan sebagai pemecah ikatan azeotrop.
Sekian penjelasan mengenai pengertian destilasi, prinsip kerja destilasi, macam macam destilasi, dan tujuan destilasi. Destilasi merupakan suatu metode yang berguna sebagai pemisah bahan kimia berdasarkan kemudahan atau perbedaan kecepatan dalam volatilitas bahan maupun menguap. Semoga artikel ini dapat bermanfaat dan terima kasih telah berkunjung di blog ini.